
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
前立腺がんとダロルタミド
2023-11-04
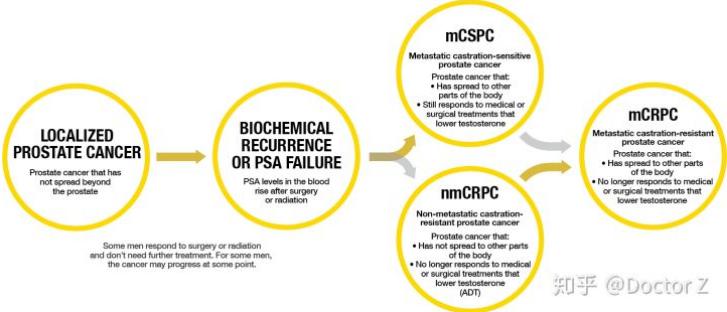
病気の背景
前立腺がんは、前立腺におけるがん細胞の制御不能な増殖によって発生します。前立腺は膀胱の下、直腸の前に位置し、男性にのみ存在します。ほぼすべての前立腺がん(原発性前立腺がんの 95% 以上)は腺細胞から発生し、腺がんとして知られています(国立がん研究所、2017)。他の種類の前立腺がん(肉腫、小細胞がん、神経内分泌腫瘍、移行上皮がんなど)も存在しますが、まれです(American Cancer Society、2016)。
世界規模で見ると、前立腺がんは男性では 2 番目に多いがんであり、全体では 4 番目に多いがんです。また、男性の癌による死亡原因の第 5 位でもあります。 2012 年、世界保健機関 (WHO) は、世界中で 110 万人の男性が前立腺がんと診断され、症例のほぼ 70% が先進地域で発生していると推定しました。生検に続く前立腺特異抗原(PSA)検査の普及により、北米、西ヨーロッパ、北欧などの先進地域では前立腺がんと診断される発生率が高くなっていますが、東部と中南部では依然として発生率が低いままです。アジア人集団 (GLOBOCAN、2012)。
前立腺がんの発症に伴う症状がないことが多いため、PSA 検査が推奨されます。ただし、前立腺がんによって症状が生じる場合があります。考えられる症状には次のようなものがあります。
•切迫感を伴う頻尿、特に夜間
•排尿の開始/停止の困難
•尿の流れが弱い
•勃起の困難
•痛みを伴う射精。射精される液体の量の減少
•排尿痛または灼熱感。血尿または精液
•腰、腰、骨盤、または大腿部の痛み。
ダロルタミドの紹介
ダロルタミドは、2019 年 7 月 30 日に FDA によって承認され、2020 年 3 月 27 日に EMA によって承認されました。商品名は Nubeqa です。この薬はオリノン社によって研究され、2014年6月にバイエル社が世界規模での開発および商業権を取得しました。その分子構造はエンザルタミドやアパルタミドとは異なり、その独特の化学構造により、この薬剤は核異所性をブロックすることでアンドロゲン受容体の機能をブロックし、がん細胞の増殖を抑制します。
Nubeqa は、非転移性去勢抵抗性前立腺がんの治療のための非ステロイド性アンドロゲン受容体阻害剤です。
Nubeqa は経口錠剤で、1 錠あたりダロルタミド 300mg を含有します。
ダロルタミドの基本情報
研究コード:ODM-201
作用機序: アンドロゲン受容体拮抗薬
研究ステータス: 承認済み
構造:
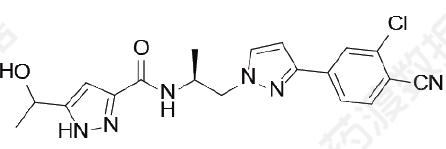
分子量:398.85
分子構造: C19H19ClN6O2
CAS : 1297538-32-9
グローカルの承認



形成不全の経路
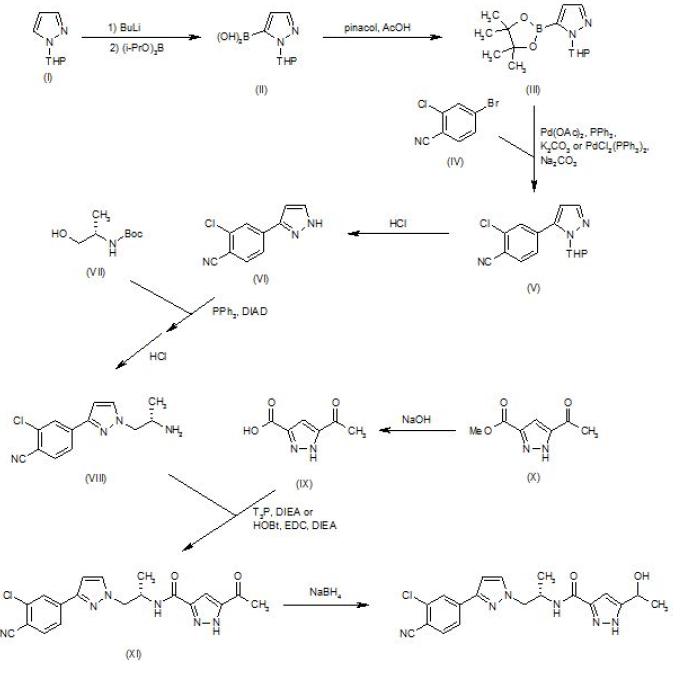
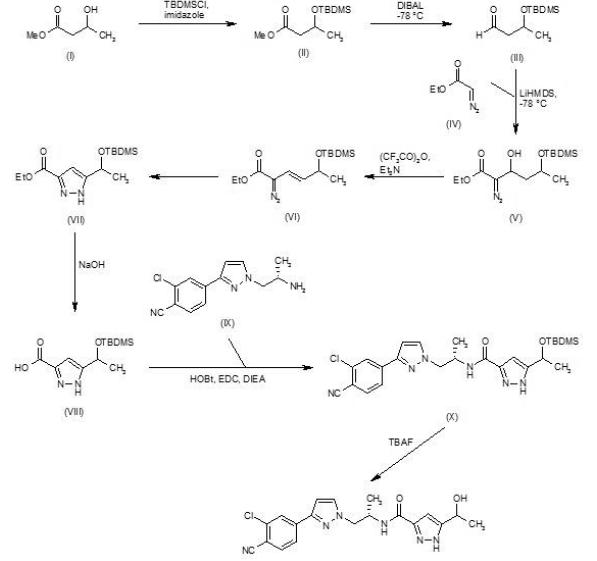
関連する中間体
| 79069-13-9 |
N-Boc-L-アラニノール |
| 1297537-37-1 |
2-クロロ-4-(1H-ピラゾール-5-イル)ベンゾニトリル |
| 1297537-41-7 |
(S)-4-(1-(2-アミノプロピル)-1H-ピラゾール-3-イル)-2-クロロベンゾニトリル |
|
1297537-45-1 |
5-アセチル-1H-ピラゾール-3-カルボン酸 |
治療分野の競合他社





